多糖结合疫苗工艺相关杂质分析
多糖结合疫苗(Polysaccharide Conjugate Vaccine),是指采用化学或其他方法将病原微生物的多糖抗原结合在载体蛋白上所制备成的多糖-蛋白结合疫苗,如b型流感嗜血杆菌多糖结合疫苗、脑膜炎球菌多糖结合疫苗和肺炎球菌多糖结合疫苗等。多糖结合疫苗的生产工艺较为复杂,主要包括以下几个关键步骤:多糖抗原制备、载体蛋白制备、多糖与载体蛋白结合以及纯化,在这些过程中均可能有多种工艺相关杂质的引入或残留,从而可能影响疫苗的安全性、免疫原性以及稳定性,因此需要对其进行研究和控制。
根据多糖结合疫苗的生产工艺,工艺相关杂质分别在多糖、载体蛋白以及多糖-蛋白结合原液三部分进行控制。
多糖
工艺相关杂质来源于发酵、杀菌以及纯化等工艺步骤,主要包括宿主来源的蛋白和核酸、发酵过程中引入的消泡剂、杀菌剂(脱氧胆酸钠或甲醛)、多糖沉淀试剂(如十六烷基三甲基溴化铵或者有机溶剂等)以及其他引入的纯化试剂。
载体蛋白
包括破伤风类毒素(TT)、白喉类毒素(DT)和突变型白喉毒素(CRM197)等,工艺相关杂质除宿主蛋白和核酸、消泡剂外,需要关注发酵过程中可能引入的诱导剂、纯化过程中添加的甲醛、沉淀剂(如硫酸铵)以及其他纯化试剂。
多糖-蛋白结合原液
工艺相关杂质研究应关注活化衍生试剂(氰基硼氢化钠、高碘酸钠、碳二亚胺等)、有机溶剂、淬灭剂(硼氢化钠)等。另外考虑加入的反应试剂多为有活性的试剂,部分试剂化学性质不稳定性,应依据试剂最终分子特性开发适宜的检测方法。
上海中科新生命生物科技有限公司具有丰富的工艺相关杂质分析经验,以下是针对多糖结合疫苗中工艺相关杂质分析的检测清单:
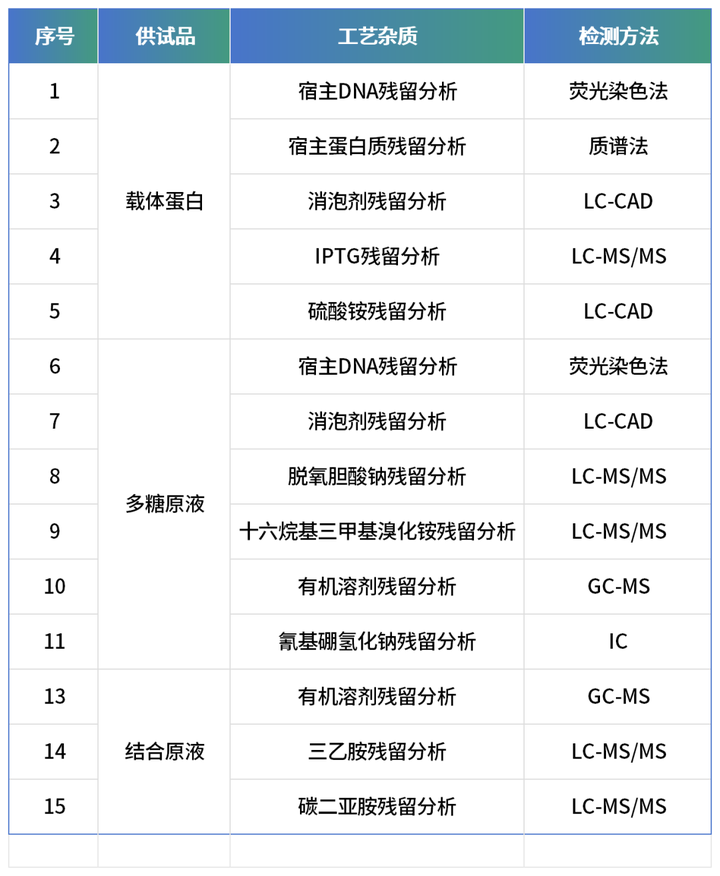
案例
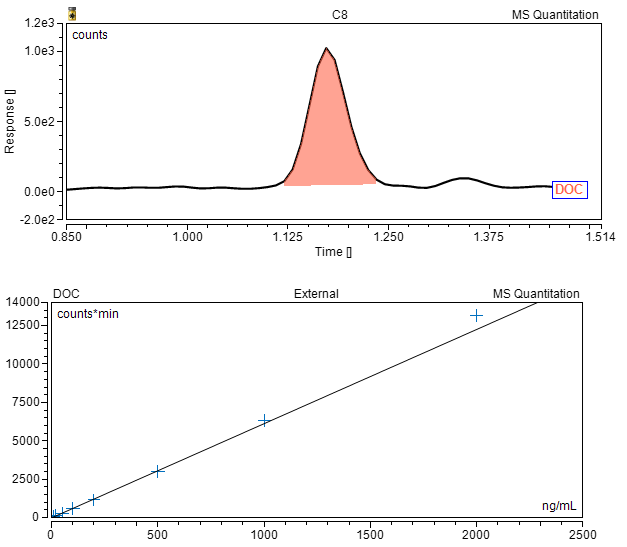
脱氧胆酸钠(DOC)检测
检测方法:LC-MS/MS; LOQ: 10ng/mL;
线性区间:10-2000ng/mL
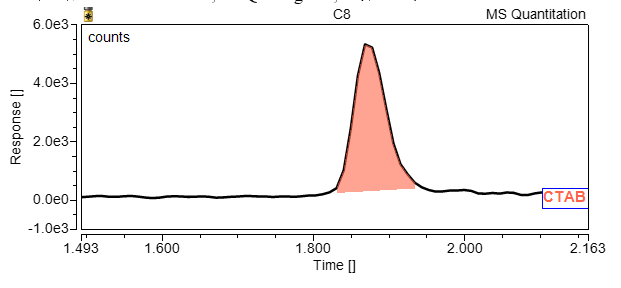
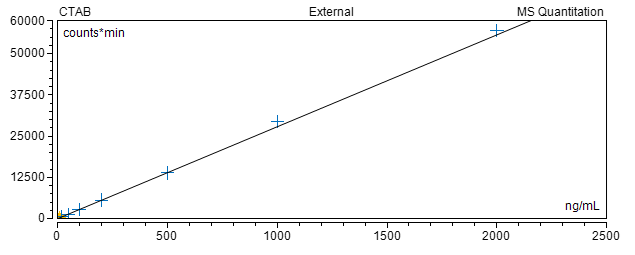
十六烷基三甲基溴化铵
(CTAB)检测
检测方法:LC-MS/MS; LOQ: 10ng/mL;
线性区间:10-2000ng/mL
参考文献
-
1. 多糖结合疫苗质量控制技术指导原则(试行)
-
2. 中国药典 2020年版



